關於樂和
乐于心,和与众,与己乐,与人和; 心宽念纯,百病无生。

癌症作為多年霸榜人類死因之首的疾病,其惡性程度已經讓人生畏,但是還有比患上癌症更可怕的事:手術無法進行;化療半劑量也無法耐受;放療不適用...
每一種治療方式的否定都在縮小患者生的希望。
比癌症更可怕的是無法可醫,還有甚麼選擇可用?癌症治療不只有“三板斧”,還有更多新療法等著你瞭解。
Overview of the illness
2024年11月,陳先生突然出現血尿,行MR檢查確診膀胱癌;PET-CT示:膀胱前上壁增厚,局部邊緣鈣化,異常代謝增高;腹膜後、兩側髂血管旁及盆壁、雙側腹股溝多發增大高代謝淋巴結;綜合考慮膀胱癌伴多發淋巴結轉移可能性大。
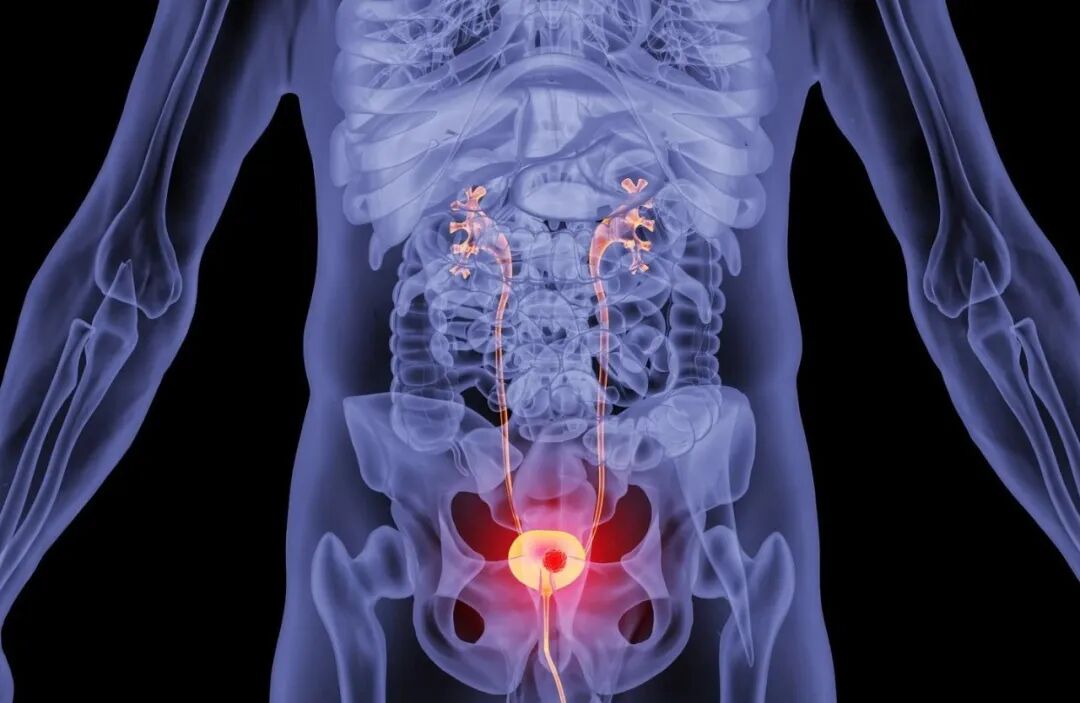
2024年12月,膀胱鏡示:膀胱多發腫瘤。三角區、左側壁、後壁、頂壁均見實性新生物,大小1-4cm不等。
病理回報:(膀胱腫瘤)低分化癌,結合免疫組化結果,考慮為膀胱高級別浸潤性尿路上皮癌,未見固有肌層,活檢組織局限,請結合臨床。
陳先生確診後本計劃2025年2月,春節後進行手術,但等待手術期間突發心臟問題,安裝了心臟起搏器,考慮到陳先生本就80歲高齡,又有基礎疾病,這讓計劃中的膀胱癌手術變得艱難不可行。
無奈,只能選擇半劑量化療,結果化療後第二天陳先生就出現高熱39~40℃,診斷為腎炎,緊急進行消炎退熱處理。不耐受,讓陳先生的化療治療路徑再次受阻。
癌症治療三板斧目前只剩下放療,但是陳先生所患的膀胱癌為多為尿路上皮癌,佔所有膀胱惡性腫瘤的90%,屬於對放療相對不敏感的實體腫瘤類型。癌細胞修復能力較強,如果使用放療需更高劑量才能達到治療效果,但高劑量可能加重正常組織損傷,副作用顯著,復發率高、遠期療效有限[1-2],醫生不建議放療。
張明徽教授團隊案例解讀
癌症治療常規三板斧都不可用,一些新的藥物和療法能不能為患者提供更多可能性?張明徽教授幫助患者從絕望中尋找希望。
陳先生的免疫組化結果提供思路:CK20(部分+),CK7(+),CK5/6(局灶+),GATA-3(部分+),p63(局灶+),HER-2(2+),NKX3.1(-),Syn(-),INSM1(-),S0X-10(-),PAX-8(-),PDL1(SP263)(CPS:25)。
HER-2(2+),這個蛋白呈現陽性,一方面意味著這個膀胱癌患者可能具有更高的惡性程度和更差的生存率;但從治療方面看,若FISH確認擴增,患者可能從抗HER-2靶向藥物中獲益。
PDL1(SP263)(CPS:25),意為每100個腫瘤細胞中有25個陽性細胞,提示腫瘤微環境中PD-L1表達較高,可能對PD-1/PD-L1抑制劑更敏感,這也許能成為陳先生治療的又一突破口。
PD-1抑制劑和PD-L1抑制劑兩者的作用原理是完全不同的:
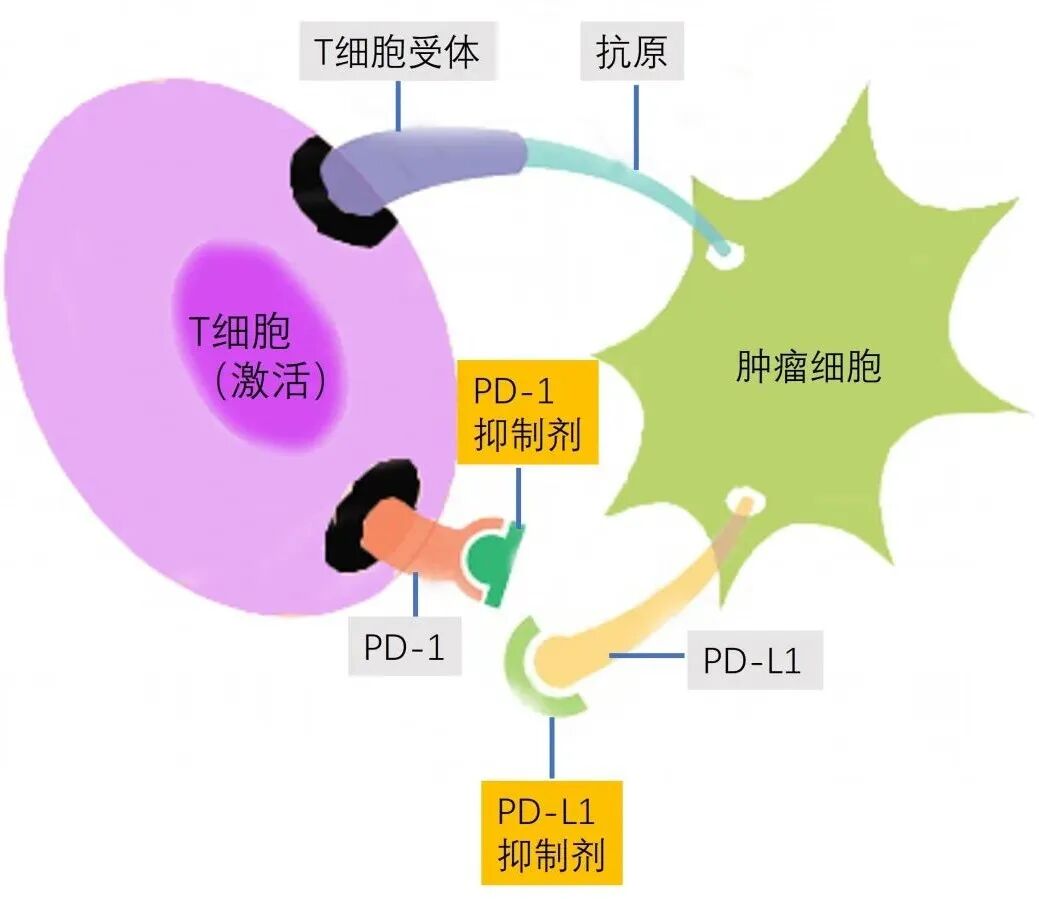
* PD-1抑制劑
屬於IgG4類抗體,結合於活化的T細胞表面的PD-1蛋白,腫瘤組織裡頭有很多淋巴細胞,這些淋巴細胞被腫瘤的PD-L1分子阻擋,使得淋巴細胞不能正常發揮作用,這時候使用PD-1抑制劑就把浸潤到腫瘤組織里的淋巴細胞重新激活,來殺傷腫瘤,但是免疫細胞一旦激活它雖然能夠殺傷腫瘤,但同時也可能導致T細胞功能衰竭,增加潛在自身免疫反應風險,產生的副作用也較多,例如甲狀腺功能低下、一型糖尿病、肺部慢性纖維化、心肌炎等等。[3-4]
* PD-L1抑制
劑屬於IgG1類抗體,主要結合於腫瘤細胞表面的PD-L1蛋白,從而促進免疫系統對腫瘤細胞的反應,是對腫瘤細胞直接殺傷,副作用較小。[3-4]
除了作用原理,臨床的實際應用中,PD-1 和 PD-L1 抑制劑的療效差別也非常明顯。PD-1抑制劑在多數癌種(如NSCLC、胃癌)中總體生存優勢更顯著,而PD-L1抑制劑在特定場景(如尿路上皮癌、聯合放療)表現更優。因此選擇需根據不同瘤種、干預類型、生物標誌物、患者基礎疾病、安全性等因素綜合考慮。
結論與點評
張明徽教授的樂和新醫團隊在綜合分析了陳先生的病情後,認為PD-L1 抑制劑更適合當前陳先生的情況,聯合前面提到的HER-2靶向藥物,後續還可以跟進vNKT免疫細胞治療、中醫等方式,通過免疫綜合治療,讓多種免疫相關藥物和手段聯合運用,以提升對複雜癌症的治療效果。

NKT細胞 (Natural killer T cell),是一種細胞表面既有T細胞受體TCR,又有NK細胞受體的特殊T細胞亞群,它兼具NK細胞和T細胞的重要特徵,具有非特異性和特異性識別腫瘤細胞的雙重能力,可以非常快速地殺傷腫瘤細胞。在NKT細胞亞群中,有一種個頭更大、殺傷能力更強的特種兵,就是清華大學張明徽教授的實驗團隊發現的vNKT(Variant Natural Killer T)細胞。
這群vNKT細胞在體內的數量非常少,且不會輕易被激活。但是一旦被活化,卻能以一當百,殺滅那些可能殘存在體內無法被發現的腫瘤細胞。另外,研究還發現vNKT細胞具有雙重抗腫瘤效應,不僅能夠直接殺傷癌細胞,還會調節腫瘤組織內部的免疫微環境,殺傷抑制性免疫細胞MDSCs,打破腫瘤的免疫逃逸,重建正常免疫系統,進一步預防復發轉移。
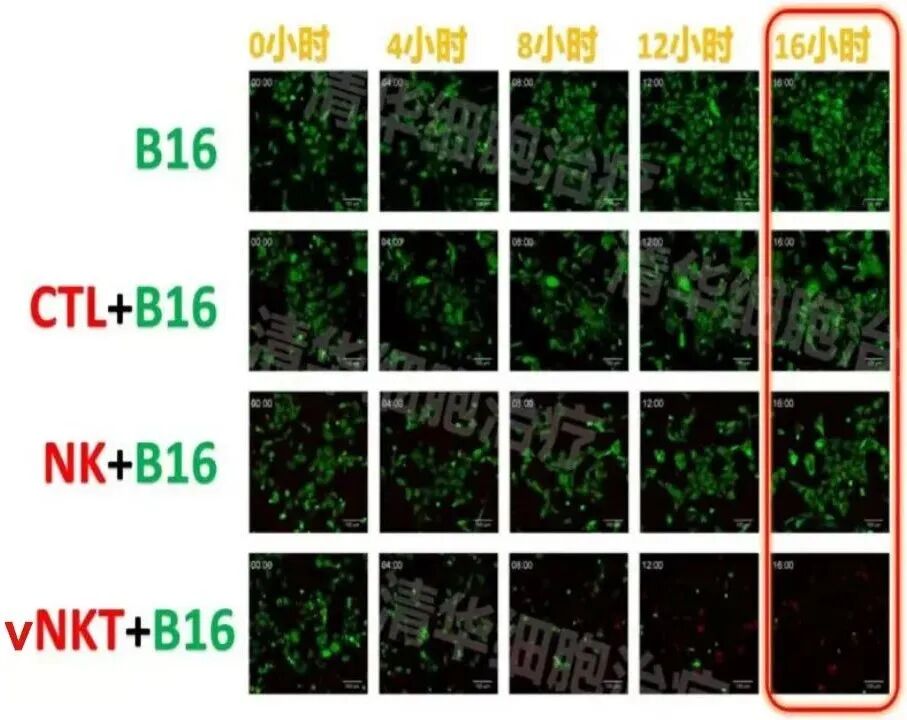
實驗條件:有vNKT細胞存在的情況下,經過16個小時,近乎所有B16腫瘤細胞被殺死!
[1]中國腫瘤醫院泌尿腫瘤協作組. 中國膀胱癌保膀胱治療多學科診治協作共識[J]. 中華腫瘤雜誌, 2022, 44(3):209-218.DOI: 10.3760/cma.j.cn112152-20220113-00035.
[2]Mohamed S.Zaghloul,John P.Christodouleas,et al.Adjuvant Sandwich Chemotherapy Plus Radiotherapy vs Adjuvant Chemotherapy Alone for Locally Advanced Bladder Cancer After Radical Cystectomy.JAMA SURGERY.November 2017 doi:10.1001/jamasurg.2017.4591
[3]Alsaab HO et al. PD-1 and PD-L1 Checkpoint Signaling Inhibition for Cancer Immunotherapy: Mechanism, Combinations, and Clinical Outcome. Front Pharmacol. 2017;8:561.
[4]Duan J et al. Use of Immunotherapy With Programmed Cell Death 1 vs Programmed Cell Death Ligand 1 Inhibitors in Patients With Cancer: A Systematic Review and Meta-analysis. JAMA Oncol. 2020;6(3):375-384.
如果您正在經歷類似的治療困境,張明徽教授的樂和新醫團隊【第二診療意見】、【癌症免疫綜合治療建議】可為您支持個性化治療方案,專業力量助力您找到最適合的生存策略。

掃描二維碼
與張明徽教授團隊溝通

樂和新醫創始人
清華大學醫學院免疫學博士,2002年發現vNKT細胞至今,張明徽教授帶領的研究團隊走過了20餘年的研究歷程,積累了700余例實體腫瘤的治療經驗,涉及幾乎所有常見實體腫瘤,研究結果充分證明vNKT在實體腫瘤治療中具有巨大價值。

適用於病理惡性程度較高或存在復發風險的術後患者;經化療、放療、靶向治療等常規治療腫瘤已基本控制但仍未達到治癒的患者;持續存在較高致癌因素的患者;放療、化療不耐受的患者。這些患者如果在傳統抗腫瘤治療後沒有進行有效的後續治療,復發、轉移或再發腫瘤將是大概率事件,在這種情況vNKT細胞治療是理想的後續治療手段,可顯著改善患者的預後。
點擊圖片查看往期精彩內容